Vacina contra Herpes Zóster Pode Entrar no SUS: Opine na Consulta Pública
O Ministério da Saúde iniciou uma consulta pública para avaliar a inclusão da vacina contra o herpes zóster no Programa Nacional de Imunização (PNI). A proposta em discussão visa beneficiar idosos com 80 anos ou mais e pessoas imunocomprometidas a partir dos 18 anos.
A Consulta Pública nº 78 está aberta para contribuições na plataforma Participa + Brasil até o dia 6 de outubro. Até o momento, a iniciativa já recebeu 75 manifestações. A participação é aberta a todos que desejam expressar suas opiniões e sugestões sobre o tema.
O herpes-zóster, também conhecido como cobreiro, é uma condição causada pela reativação do vírus da catapora (varicela-zóster), afetando principalmente idosos e pessoas com baixa imunidade. A doença é caracterizada por dor intensa, febre, erupções cutâneas e bolhas, podendo levar a complicações graves, como a neuralgia pós-herpética (NPH), uma dor crônica persistente.
Entre 2008 e 2024, o Sistema Único de Saúde (SUS) registrou mais de 85 mil atendimentos ambulatoriais e 30 mil internações decorrentes do herpes-zóster no Brasil. No período de 2007 a 2023, foram registradas 1.567 mortes associadas à doença, a maioria em indivíduos com 50 anos ou mais.
Atualmente, o tratamento oferecido pelo SUS para herpes-zóster inclui medicamentos para aliviar os sintomas e, em casos mais graves, antivirais como o aciclovir. Para a NPH, são disponibilizados fármacos como amitriptilina, carbamazepina e lidocaína em gel.
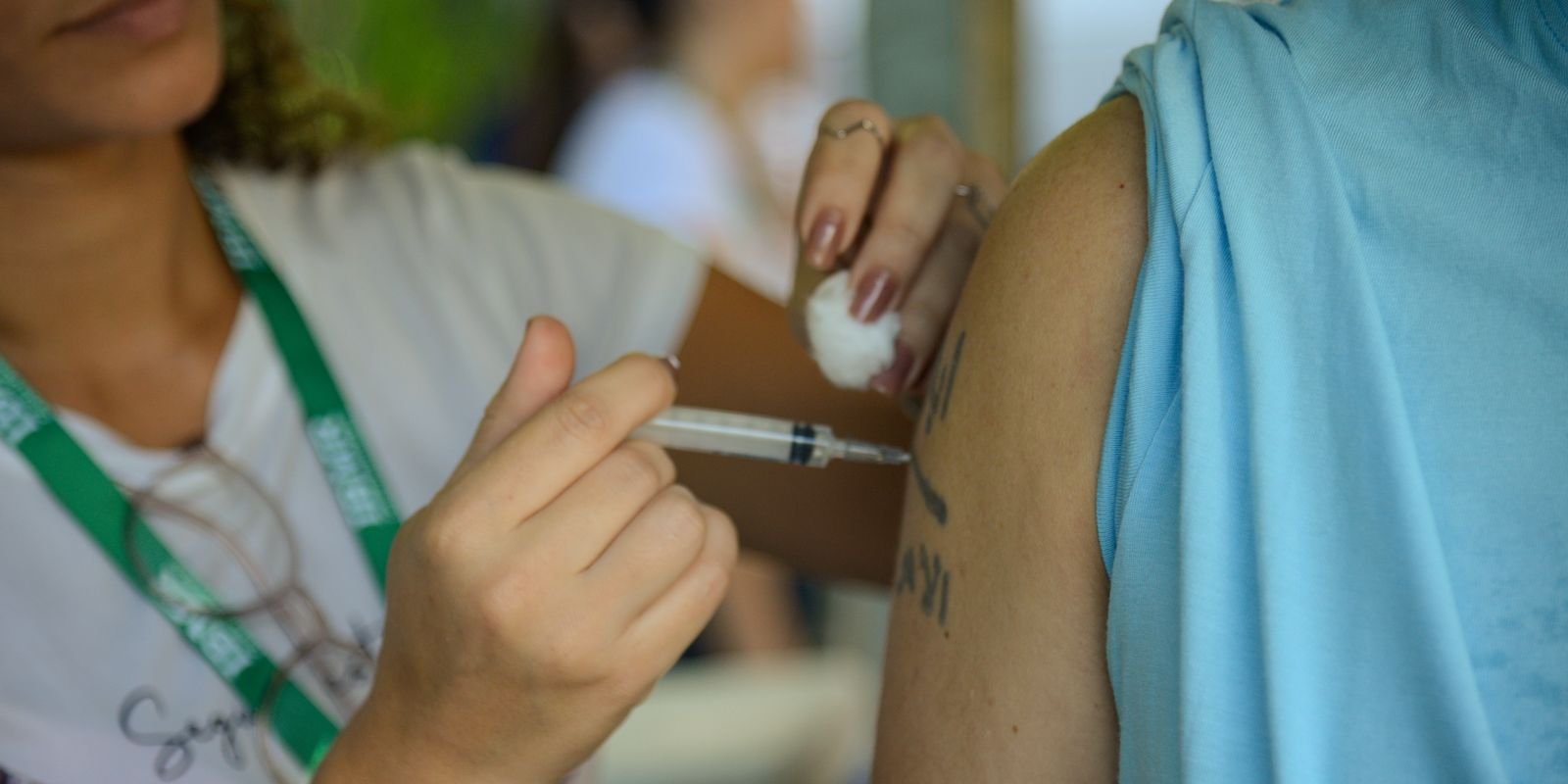
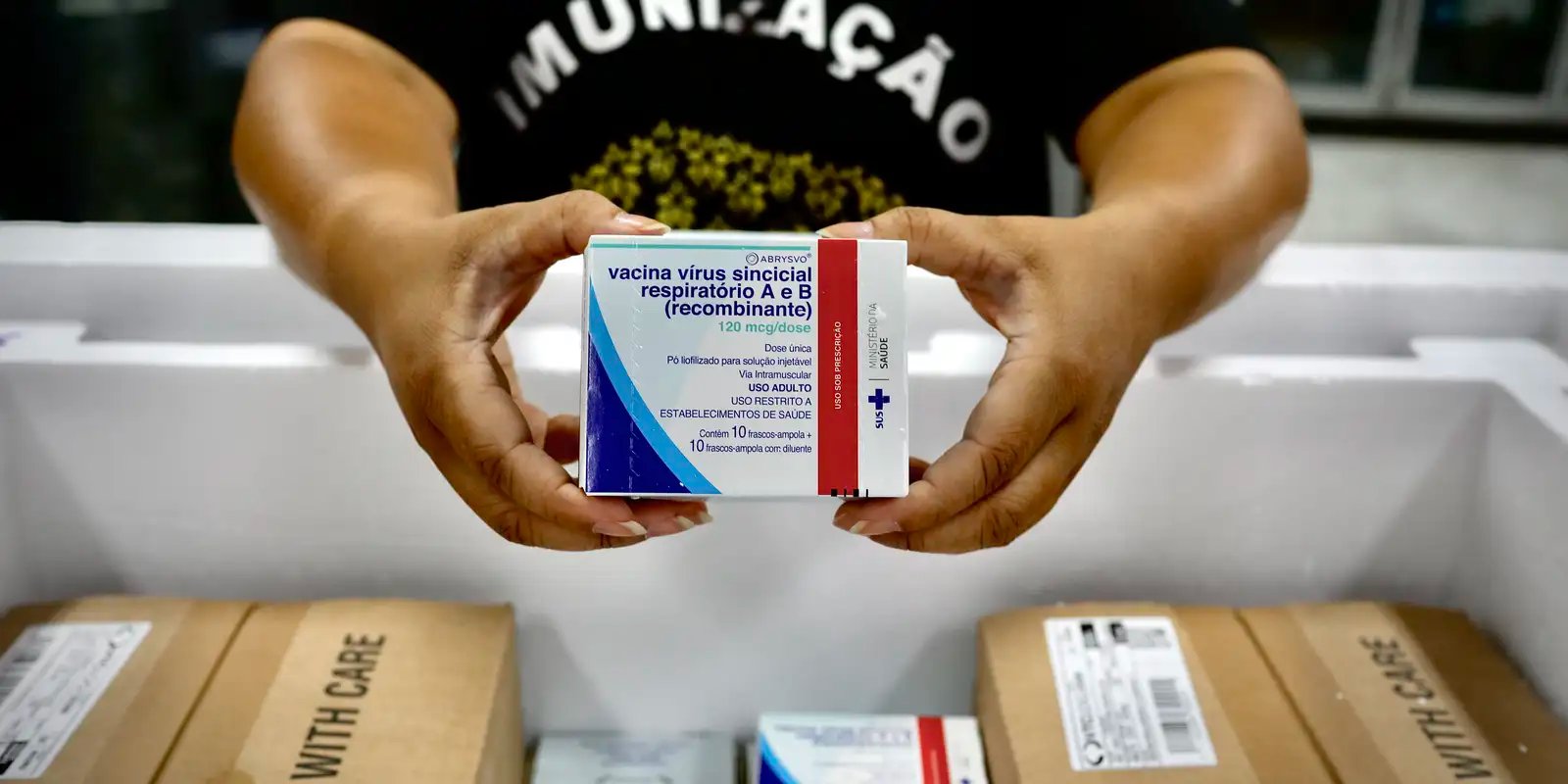
A incorporação da vacina recombinante adjuvada foi solicitada pelo Departamento do Programa Nacional de Imunizações, da Secretaria de Vigilância em Saúde e Ambiente, e do Ministério da Saúde. A vacina, administrada em duas doses intramusculares com intervalo de dois meses, contém uma proteína do vírus varicela-zóster (antígeno gE) combinada a um adjuvante (AS01B) para estimular o sistema imunológico.
Estudos avaliados pela Comissão Nacional de Incorporação de Tecnologias (Conitec) indicam que a vacina apresenta eficácia superior a 80% na prevenção da doença e da NPH. Os eventos adversos mais comuns relatados incluem dor no local da aplicação, fadiga, dor muscular, cefaleia e febre, geralmente de intensidade leve a moderada. A vacina também foi considerada segura.
O principal obstáculo para a incorporação é o alto custo, com um investimento estimado em R$ 5,2 bilhões ao longo de cinco anos. A Conitec concluiu que a vacina não oferece um benefício suficientemente significativo para justificar o custo para o SUS. As contribuições da consulta pública serão analisadas pela comissão técnica, que tomará a decisão final sobre a inclusão da vacina no PNI.
Fonte: agenciabrasil.ebc.com.br
Share this content:












Publicar comentário